验厂认证联盟欢迎您!
- 微信公众号

扫一扫关注
- 联系电话:13602503249
- 联系客服

扫一扫关注

♛办理条件/Conditions 申请人应为境内依法进行登记的企业 ۞申请材料清单/List of application materials 1.申请表 2.证明性文件 (1)企业营业执照副本复印件。 (2)组织机构代码证复印....
0755-86610833 立即咨询申请人应为境内依法进行登记的企业
1.申请表
2.证明性文件
(1)企业营业执照副本复印件。
(2)组织机构代码证复印件。
3.注册人关于变更情况的声明
4.原医疗器械注册证及其附件复印件、历次医疗器械注册变更文件复印件
5.变更申请项目申报资料要求
根据具体变更情况选择提交以下文件:
(1)产品名称变化的对比表及说明。
(2)产品技术要求变化的对比表及说明。
(3)型号、规格变化的对比表及说明。
(4)结构及组成变化的对比表及说明。
(5)产品适用范围变化的对比表及说明。
(6)进口医疗器械生产地址变化的对比表及说明。
(7)注册证中“其他内容”变化的对比表及说明。
(8)其他变化的说明。
6.与产品变化相关的安全风险管理报告
7.变化部分对产品安全性、有效性影响的资料分析并说明变化部分对产品安全性、有效性的影响,并提供相关的研究资料。适用范围变化的必须提供临床评价资料。
8.针对产品技术要求变化部分的注册检验报告
9.符合性声明
(1)注册人声明本产品符合《医疗器械注册管理办法》和相关法规的要求;声明本产品符合现行国家标准、行业标准,并提供符合标准的清单。
(2)所提交资料真实性的自我保证声明。
|
名称 |
解释说明 |
时限 |
|
受理 |
|
5(工作日) |
|
行政许可决定 |
20个工作日(不含技术审评和申请人补充资料及补充资料审评所需的时间)。20个工作日内不能做出决定的,经局领导批准,可延长10个工作日。 |
20(工作日) |
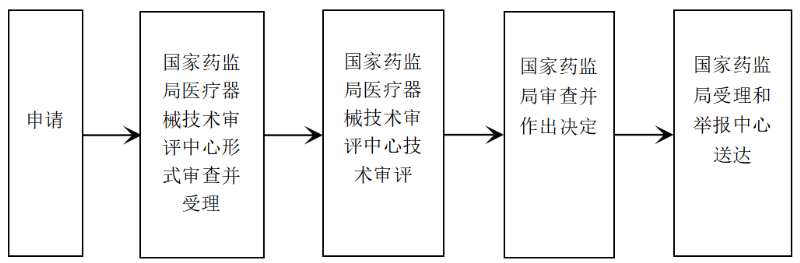
♛办理条件/Conditions 办理医疗器械注册证----申请人应为境内依法进行登记的企业 ۞申请材料清单/List of application materials 1.申请表 2.证明性文件 3.医疗器械安全有效基本要求清单...

一、办理要素 (一)事项名称和编码:二、三类医疗器械生产企业委托生产备案,(A138-000) (二)受理范围 1.申请人:广东省内具有医疗器械生产许可资格的企业 2.申请内容:二、三类...

首次注册提交材料 资料编号(一) 境内第三类医疗器械注册申请表; 资料编号(二) 医疗器械生产企业资格证明; 资料编号(三) 产品技术报告; 资料编号(四) 安全风险分析报告; 资料编...