验厂认证联盟欢迎您!
- 微信公众号

扫一扫关注
- 联系电话:13602503249
- 联系客服

扫一扫关注

♛办理条件/Conditions 国家食品药品监督管理局发布的第一类医疗器械产品目录和相应体外诊断试剂分类子目录中的第一类医疗器械。 ۞申请材料清单/List of application materials 1、一....
0755-86610833 立即咨询国家食品药品监督管理局发布的第一类医疗器械产品目录和相应体外诊断试剂分类子目录中的第一类医疗器械。
|
1、一类医疗器械备案表 2、安全风险分析报告 3、产品技术要求 4、产品检验报告 5、临床评价资料 6、产品说明书及最小销售单元标签设计样稿 |
8、营业执照(A类有限责任公司)
9、符合性声明
10、授权委托书
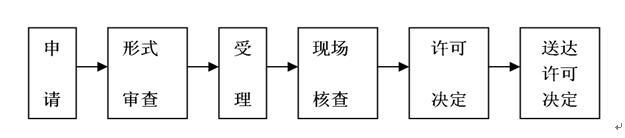
|
名称 |
其他 |
时限 |
|
法定办结时限 |
办理医疗器械备案,备案人应当按照《医疗器械监督管理条例》第九条的规定提交备案资料。 |
1(工作日) |
|
承诺办结时限 |
办理医疗器械备案,备案人应当按照《医疗器械监督管理条例》第九条的规定提交备案资料。 |
1(工作日) |
| 到现场次数 | 0次 |
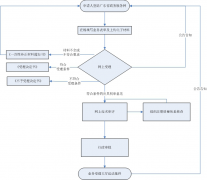
♛办理条件/Conditions 1、申报注册的产品为按医疗器械管理的体外诊断试剂,且已经列入《体外诊断试剂分类子目录》,管理类别为第二类。(注:对新研制的尚未列入分类目录的...

第一类医疗器械备案申报要求 申请材料目录: 1、第一类医疗器械备案表; 2、安全风险分析报告; 3、产品技术要求; 4、产品检验报告; 5、临床评价资料; 6、产品说明书及最...

第一类医疗器械生产备案要求 申请材料目录: 1.第一类医疗器械生产备案表; 2.所生产产品的医疗器械备案凭证复印件; 3.经备案的产品技术要求复印件; 4.营业执照和组织机构...